EE. UU. autoriza vacunación en embarazadas
Esta inyección, administrable entre las semanas 32 y 36 de gestación, garantiza la protección de los bebés durante sus primeros seis meses de vida contra el VRS.
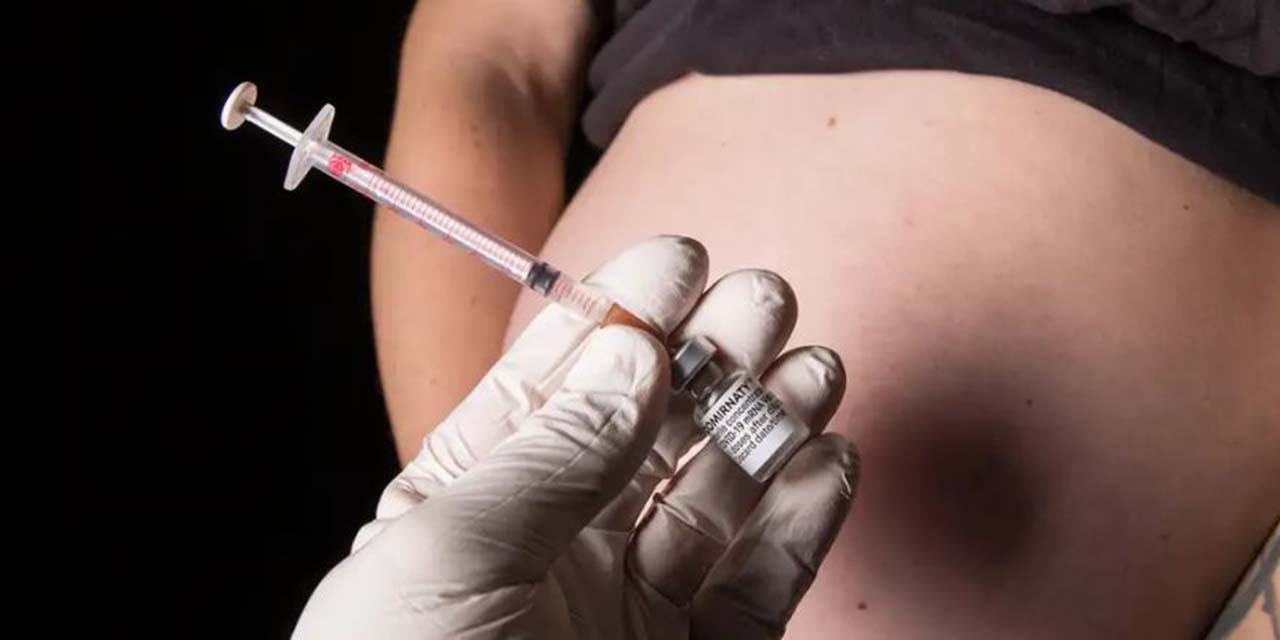
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos dio luz verde a una vacuna de Pfizer destinada a mujeres embarazadas, con el propósito específico de proteger a los neonatos del virus respiratorio sincitial (VRS).
Esta inyección, administrable entre las semanas 32 y 36 de gestación, garantiza la protección de los bebés durante sus primeros seis meses de vida contra el VRS. Según datos de la FDA, el VRS es el principal agente causal de hospitalizaciones de lactantes en el país.
Aunque esta vacuna, llamada Abrysvo, ya había sido autorizada en mayo para adultos mayores de 60 años, la nueva aprobación marca un paso significativo en la prevención de la enfermedad en lactantes. Paralelamente, otro preparado similar denominado Arexvy obtuvo en julio el aval de la Agencia Europea del Medicamento (EMA), cubriendo tanto a neonatos como a personas de la tercera edad. Sin embargo, su introducción al mercado europeo todavía está pendiente de aprobación por parte de la Comisión Europea.
Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA, destacó la relevancia del virus en la población infantil. Marks recalcó: “Es una causa común de enfermedad en los niños, siendo los lactantes los más susceptibles a formas graves que requieren hospitalización”.
Las pruebas clínicas, en las que participaron cerca de 7.000 mujeres embarazadas, reflejaron la eficacia de Abrysvo, mostrando una reducción del 82% en las manifestaciones graves de la enfermedad en neonatos de 0 a 3 meses y del 69% en infantes de hasta 6 meses. Es preciso señalar que, aunque el VRS suele manifestarse como un simple resfriado en niños, puede complicarse hasta causar neumonía o bronquiolitis.
Estimaciones de los Centros para el Control y la Prevención de Enfermedades (CDC) indican que anualmente entre 58.000 y 80.000 niños menores de cinco años son hospitalizados a causa del VRS.
A pesar de los prometedores resultados, se registraron efectos secundarios en algunas mujeres vacunadas con Abrysvo, incluyendo molestias en el punto de inyección, cefaleas, dolores musculares y náuseas. Además, se notó un ligero incremento en la aparición de preeclampsia y partos prematuros comparado con el grupo que recibió un placebo.
Por ello, la FDA ha solicitado a Pfizer continuar investigando estos posibles riesgos. La aprobación definitiva del producto por parte de los CDC aún está pendiente, lo que genera incertidumbre sobre su disponibilidad para la próxima temporada de VRS.









